Erfolgreich: Freiwilliges Harmonisierungsverfahren klinischer Prüfungen in Europa trägt Früchte
Unter Federführung des Paul-Ehrlich-Instituts (PEI) ging vor drei Jahren das freiwillige Harmonisierungsverfahren für klinische Prüfungen an den Start (VHP, Voluntary Harmonisation Procedure). Es ermöglicht Antragstellern, das Verfahren zur Genehmigung klinische Prüfungen mit einem Antrag gleichzeitig in mehreren europäischen Ländern zu starten. Die Bilanz nach drei Jahren ist sehr positiv: Die Zeitspanne bis zur Genehmigung einer multinationalen klinischen Prüfung in allen beteiligten EU-Staaten konnte auf unter drei Monate gesenkt werden. Über die bisherigen Erfahrungen und geplante weitere Schritte berichten Experten des PEI in der Online-Ausgabe von Nature Reviews Drug Discovery vom 10. April 2012 (doi:10.1038/nrd3202-c2)
Die Entwicklung neuer und innovativer Arzneimittel ist ein langwieriger Prozess. Nach der präklinischen Entwicklungsphase müssen Arzneimittelkandidaten in einer Reihe klinischer Prüfungen auf ihre Wirksamkeit und Unbedenklichkeit geprüft werden. In jedem europäischen Land, in dem eine solche klinische Prüfung durchgeführt werden soll, bedarf es einer nationalen Genehmigung. Sollte eine Studie in mehreren Ländern Europas durchgeführt werden, bedeutete dies lange Zeit, dass sie in jedem Land erneut das gesamte Verfahren der Validierung, Bewertung, Mängelbehebung und Genehmigung/Ablehnung durchlaufen musste. Bei einer großen multinationalen Studie mit mehr als zehn Mitgliedstaaten konnte - und kann - die Genehmigung in allen Ländern leicht mehr als ein Jahr dauern.
Hier Abhilfe zu schaffen, nahm sich die 'Clinical Trials Facilitation Group' (CTFG), eine Arbeitsgruppe der HMA ('Heads of Medicines Agencies'), vor. Sie entwickelte unter Federführung von Experten des Paul-Ehrlich-Instituts (PEI) ein Verfahren, das sowohl für Antragsteller als auch für die Arzneimittelagenturen in Europa einen großen Fortschritt darstellt: Das freiwillige Harmonisierungsverfahren‚ 'Voluntary Harmonisation Procedure' (VHP). Seit März 2009 bietet die CTFG damit Antragstellern, die eine klinische Prüfung in drei oder mehr EU-Mitgliedstaaten durchführen möchten, die Möglichkeit, mit einem einzigen Antrag ein Genehmigungsverfahren in diesen Ländern zu starten. "Die Prüfung und Bewertung klinischer Studien ist von zentraler Bedeutung für die Entwicklung neuer Arzneimittel. Diese Verfahren in Europa zu harmonisieren und so zu einer Beschleunigung bei gleichzeitig größter Sorgfalt bei der Bewertung zu sorgen, ist uns im PEI ein großes Anliegen. Ich freue mich, dass das Paul-Ehrlich-Institut hier eine führende Rolle übernommen hat"
, sagt Prof. Klaus Cichutek, Präsident des Paul-Ehrlich-Instituts.
Eine aktuelle Auswertung zeigt, dass das Verfahren die Genehmigung multinationaler klinischer Studien tatsächlich deutlich beschleunigt hat: Im Jahr 2011 betrug die mittlere Zeitspanne bis zur Genehmigung einer multinationalen klinischen Prüfung nur noch 82 Tage. Vorher konnte dies einige Monate bis hin zu mehr als einem Jahr dauern. Dabei benötigt das eigentliche Harmonisierungsverfahren im Mittel nur ca. 50 Tage. Die Antragsteller sind gehalten, nach der positiven Bewertung der Unterlagen innerhalb der folgenden 20 Tage die Genehmigung in den einzelnen Ländern, in denen die Studie durchgeführt werden soll, zu beantragen. Die Frist für die Genehmigung liegt dort bei nur noch zehn Tagen – was möglich ist, weil alle wissenschaftlichen Fragen bereits im neuen harmonisierten Verfahren geklärt wurden. Dass sich die Zeitspanne bis zur Genehmigung multinationaler klinischer Prüfungen in den drei Jahren von 124 Tagen im ersten Jahr auf inzwischen 82 Tagen reduziert hat, liegt daran, dass das Harmonisierungsverfahren bereits mehrere Überarbeitungen erfahren hat – ein Vorteil dieses freiwilligen Verfahrens, das keiner Gesetzesänderung bedarf und bei dem sinnvolle Änderungen recht kurzfristig umgesetzt werden können.
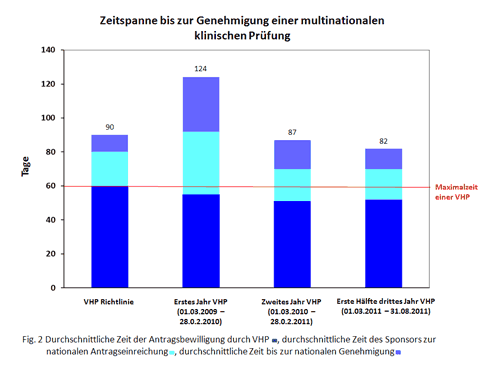 Zeitspanne bis zur Genehmigung einer multinationalen klinischen Prüfung
Quelle: PEI
Zeitspanne bis zur Genehmigung einer multinationalen klinischen Prüfung
Quelle: PEI
"Das Verfahren ist eine wichtige Vereinfachung für Antragsteller und bewertende Arzneimittelagenturen. Die Verfahren selbst werden beschleunigt, Ressourcen der Beteiligten werden optimal eingesetzt und nicht durch doppelte Arbeit belastet"
, erläutert Dr. Hartmut Krafft, Vorsitzender der CTFG. Er muss es wissen, denn Experten des PEI koordinieren alle Harmonisierungsverfahren, unabhängig davon, ob die klinischen Prüfungen in Deutschland durchgeführt werden oder nicht.
Die Zahl der Anträge nimmt zu: Im Jahr 2009 wurden 26 Anträge gestellt, in 2011 waren es bereits 85 Anträge und die Anzahl steigt weiter. Insgesamt wurden bisher 170 Anträge gestellt. Während nach VHP-Einführung zunächst vor allem universitäre Einrichtungen und kleine Unternehmen das Verfahren nutzten, wird das Angebot inzwischen auch von großen Pharmaunternehmen geschätzt – und dies über Europa hinaus: Mehr als 40 Prozent der Anträge kommen von Antragstellern mit Firmensitz in den USA.
Auch die Europäische Kommission sieht die Notwendigkeit, die Verfahren zu harmonisieren. Für Mitte 2012 wird ein Entwurf für eine neue Richtlinie zur klinischen Prüfung erwartet.
Originalpublikation
Krafft H, Bélorgey C, Szalay G (2012): Experience and further development with the Voluntary Harmonization Procedure for multinational clinical trials in the European Union.
Nat Rev Drug Discov 11: 419.
Online-Abstract
Pressekontakt:
Paul-Ehrlich-Institut
Pressestelle
Dr. Susanne Stöcker, Dr. Corinna Volz-Zang, Brigitte Morgenroth
Paul-Ehrlich-Straße 51-59
63225 Langen
GERMANY
Telefon: +49 6103 77 1030
Telefax: +49 6103 77 1262
E-Mail: Presse@pei.de
nach oben



