Einreichung im eCTD-Format
Einreichung im eCTD-Format
Das Paul-Ehrlich-Institut (PEI) bevorzugt elektronische Einreichungen für alle Verfahren im eCTD-Format, da nur in diesem Format der Lebenszyklus des Dossiers entsprechend abgebildet werden kann.
Erfolgen zu einem Produkt Einreichungen im eCTD-Format, werden auch alle Folgeeinreichungen in diesem Format erwartet. Eine Mischeinreichung eCTD / NeeS ist nicht möglich, da dann ein Lifecycle Management der Dokumentation unmöglich wird ("once eCTD always eCTD").
Beim Wechsel des Einreichungsformats von Papier oder NeeS zu eCTD (z. B. anlässlich einer Zulassung, Verlängerung oder Änderungsanzeige) bitten wir um Einreichung einer sogenannten Baseline (Sequenz 0000) für dieses Produkt. Sie umfasst mindestens die Module 1 und 3 und stellt eine große Hilfe für den Bewertungsprozess dar.
Aufbau und Benennung der eCTD-Verzeichnisstruktur
Im Namen des Root-Verzeichnisses sollte der Name des Arzneimittels bzw. die Verfahrensnummer oder beides oder als weitere Alternative die Zulassungsnummer angegeben werden. Die Benennung soll die Produktstruktur informativ berücksichtigen.
Bevorzugte Benennung
 Quelle: PEI
Quelle: PEI
Alternative Möglichkeiten
 Quelle: PEI
Quelle: PEI
 Quelle: PEI
Quelle: PEI
 Quelle: PEI
Quelle: PEI
Unterhalb des Root-Verzeichnisses werden die Sequenzordner der Einreichung (<sequence>) sowie separate Ordner für so genannte Arbeitsdokumente (<sequence>-working documents) angelegt. Diese entsprechen den in der AMG-EV festgelegten Dokumenten zur minimalen elektronischen Einreichung (entsprechend Modul 1.3.1 und Modul 2) und sind als rtf-Dokumente einzureichen.
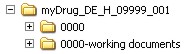 Quelle: PEI
Quelle: PEI
Betrifft die Einreichung mehrere Zulassungsanträge oder erteilte Zulassungen (z. B. zu einem Worksharing-Verfahren), sind entsprechende Verzeichnisse nach oben genanntem Bezeichnungsschema zu bilden.
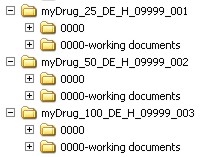 Quelle: PEI
Quelle: PEI
Werden mehrere Sequenzen auf einmal eingereicht, sind entsprechende Verzeichnisse für jede Sequenz nach folgendem Schema anzulegen:
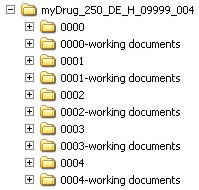 Quelle: PEI
Quelle: PEI
Innerhalb der Sequenz müssen jeweils Unterordner für die Module, ein util-Verzeichnis mit den genutzten Schemata, ein valider XML-Backbone sowie die zugehörige md5-Prüfsumme vorhanden sein.
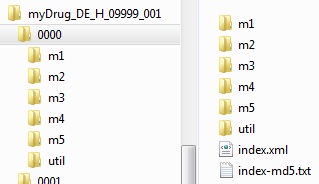 Quelle: PEI
Quelle: PEI
EU Module 1 –Inhalte des EU-Envelopes
Bei allen eCTD-Einreichungen sind in der XML-Struktur zu Modul 1 innerhalb des eu-envelope folgende Elemente und Attribute zu füllen:
| Element | Attribut | Beispiel |
| submission | type | var-type2 |
| number | | EMA/H/xxxx/WS/001 |
| tracking number | | EMA/H/C/0123/WS005/045 |
| applicant | | PharmaCompany Ltd. |
| agency | code | DE-PEI |
| invented-name | | myDrug |
| sequence | | 0000 |
| submission-description | | Responses to Day 120 List of Questions |
nach oben
Elektronische Einreichung im NeeS-Format
Elektronische Einreichung im NeeS-Format
Das Paul-Ehrlich-Institut (PEI) bevorzugt Einreichungen im eCTD-Format, da nur in diesem Format der Lebenszyklus des Dossiers entsprechend abgebildet werden kann. Daneben werden aber weiterhin elektronische Einreichungen unter Anwendung der NeeS-Guideline, das heißt ohne den XML-Backbone des eCTD-Formats, akzeptiert.
Bitte beachten Sie, dass das NeeS-Format nicht im zentralisierten Verfahren verwendet werden kann.
Beim Wechsel des Einreichungsformats von Papier zu NeeS (z. B. anlässlich einer Zulassung, Verlängerung oder Änderungsanzeige) bitten wir um Einreichung einer sogenannten Baseline (Sequenz 0000) für dieses Produkt. Sie umfasst mindestens die Module 1 und 3 und stellt eine große Hilfe für den Bewertungsprozess dar.
Aufbau und Benennung der NeeS-Verzeichnisstruktur
Im Namen des Root-Verzeichnisses sollte der Name des Arzneimittels bzw. die Verfahrensnummer oder beides oder als weitere Alternative die Zulassungsnummer angegeben werden. Die Benennung soll die Produktstruktur informativ berücksichtigen.
Bevorzugte Benennung:
 Quelle: PEI
Quelle: PEI
Alternative Möglichkeiten:
 Quelle: PEI
Quelle: PEI
 Quelle: PEI
Quelle: PEI
 Quelle: PEI
Quelle: PEI
Unterhalb des Root-Verzeichnisses werden die Sequenzordner der Einreichung (<sequence>) sowie separate Ordner für so genannte Arbeitsdokumente (<sequence>-working documents) angelegt. Diese entsprechen den in der AMG-EV festgelegten Dokumenten zur minimalen elektronischen Einreichung (entsprechend Modul 1.3.1 und Modul 2) und sind als rtf-Dokumente einzureichen.
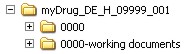 Quelle: PEI
Quelle: PEI
Betrifft die Einreichung mehrere Zulassungsanträge oder erteilte Zulassungen (z. B. zu einem Worksharing-Verfahren), sind entsprechende Verzeichnisse nach oben genanntem Bezeichnungsschema zu bilden.
 Quelle: PEI
Quelle: PEI
Werden mehrere Sequenzen auf einmal eingereicht, sind entsprechende Verzeichnisse für jede Sequenz nach folgendem Schema anzulegen:
 Quelle: PEI
Quelle: PEI
In diesem Zusammenhang wird auch die fortlaufende Nummerierung der Sequenzen eines Dossiers empfohlen. Dies vermeidet Probleme mit der zeitlichen Einordnung im Rahmen des Bewertungsprozesses.
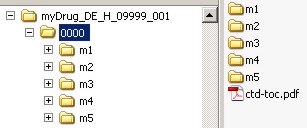
Innerhalb der Sequenz müssen jeweils Unterordner für die Module und ein Inhaltsverzeichnis "ctd-toc.pdf" vorhanden sein.
 Quelle: PEI
Quelle: PEI
nach oben
Elektronische Einreichung im vNeeS-Format
Elektronische Einreichung im vNeeS-Format
Das Paul-Ehrlich-Institut (PEI begrüßt die Verwendung des vNeeS-Formats für Einreichungen im Bereich der immunologischen Veterinärarzneimittel.
Informationen zur Strukturierung und Formatierung von Einreichungen im vNeeS-Format werden auf der eSubmission-Webseite der Europäischen Arzneimittelagentur EMA zur Verfügung gestellt.
Beim Wechsel des Einreichungsformats von Papier zu vNeeS (z. B. anlässlich einer Zulassung, Verlängerung oder Änderungsanzeige) bitten wir um Einreichung einer sogenannten Baseline (Sequenz 0000) für dieses Produkt. Sie umfasst mindestens die Teile 1 und 2 und stellt eine große Hilfe für den Bewertungsprozess dar.
Aufbau und Benennung der vNeeS-Verzeichnisstruktur
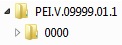
Im Namen des Root-Verzeichnisses sollte der Name des Arzneimittels bzw. die Verfahrensnummer oder beides oder als weitere Alternative die Zulassungsnummer angegeben werden. Die Benennung soll die Produktstruktur informativ berücksichtigen.
Bevorzugte Benennung
 Quelle: PEI
Quelle: PEI
Alternative Möglichkeiten
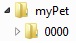 Quelle: PEI
Quelle: PEI
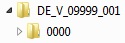 Quelle: PEI
Quelle: PEI
 Quelle: PEI
Quelle: PEI
Unterhalb des Root-Verzeichnisses werden die Sequenzordner der Einreichung (<sequence>) angelegt.
Betrifft die Einreichung mehrere Zulassungsanträge oder erteilte Zulassungen (z. B. zu einem Worksharing-Verfahren), sind entsprechende Verzeichnisse nach oben genanntem Bezeichnungsschema zu bilden.
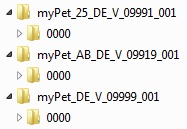 Quelle: PEI
Quelle: PEI
Werden mehrere Sequenzen auf einmal eingereicht, sind entsprechende Verzeichnisse für jede Sequenz nach folgendem Schema anzulegen:
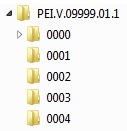 Quelle: PEI
Quelle: PEI
In diesem Zusammenhang wird auch die fortlaufende Nummerierung der Sequenzen eines Dossiers empfohlen. Dies vermeidet Probleme mit der zeitlichen Einordnung der Einreichungen im Rahmen des Bewertungsprozesses.
Innerhalb der Sequenz müssen jeweils Unterordner für die Module, für zusätzliche Arbeitsdokumente und ein Inhaltsverzeichnis "gtoc.pdf" vorhanden sein.
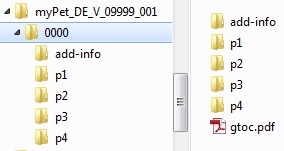 Quelle: PEI
Quelle: PEI
nach oben
Technische Validierung
Technische Validierung
Vor der Einreichung eines Dossiers empfehlen wir, eine technische Validierung durchzuführen. So können Sie feststellen, ob Ihr Dossier den genannten Anforderungen (z.B. ICH M2 eCTD v.3.2.2, EU M1 v.2.0; File and folder structure and naming conventions, PDF configurations) tatsächlich entspricht oder vorher noch Fehler zu beseitigen sind.
Mehrere Softwarehersteller bieten kostenlose Prüfprogramme (sog. Validatoren), die die derzeitigen Spezifikationen für eCTD (EU M1 v2.0 sowie ICH eCTD v. 3.2.2; EU eCTD Validation Criteria v5.0), NeeS (EU NeeS Validation Criteria v4.0) und vNeeS (vNeeS Validation Checklist v2.2) berücksichtigen. Technischer Support für die Nutzung dieser Validatoren kann von Seiten des Paul-Ehrlich-Instituts (PEI) leider nicht gegeben werden.
Das PEI wird in jedem Fall eine technische Validierung auch selbst durchführen. Antragstellende werden über das Ergebnis immer nur dann informiert, wenn Fehler im Rahmen der Pass/Fail-Kriterien aufgetreten sind. Die Angabe Ihrer E-Mail-Adresse bei Einreichung erleichtert die Zusendung des Validierungsberichtes. Warnungen im Best Practice-Bereich werden nicht kommuniziert.
Fehler führen dazu, dass eine Einreichung nicht importiert werden kann und Sie als Antragsteller aufgefordert werden, die Fehler zu beseitigen und die Sequenz neu einzureichen.
Warnungen im Best Practice-Bereich werden toleriert. Sie zeigen jedoch an, dass vorgegebene Anforderungen nicht eingehalten werden.
Fristen können erst nach einer erfolgreichen technischen Validierung gestartet werden.
nach oben